Bildnachweis: musa – stock.adobe.com, stock3.com.
Das Spezialpharmaunternehmen Clinuvel ist gut ins Geschäftsjahr 2025 gestartet und treibt seine Entwicklung aggressiv voran. So konnten im ersten Halbjahr 2025 (abgelaufenes Geschäftsjahr endete am 30. Juni 2024) die Gesamteinnahmen um 7,6 Millionen AUD auf 43,4 Millionen AUD (rund 24,9 Millionen EUR) gesteigert werden – die entspricht einem Zuwachs von 21,1 Prozent im Vergleich zum Vorjahreszeitraum. Der Gewinn pro Aktie stieg im besagten Zeitraum um 27,4 Prozent auf 28,1 australische Cents pro Aktie, während die Barreserven auf 198,2 Millionen AUD (+7,8 %; ca. 113,5 Millionen EUR) weiter ausgebaut wurden. Damit sieht man sich gut gerüstet, den eingeschlagenen Expansionspfad in Richtung „Schlüsselakteur in der Photomedizin“ weiterzuverfolgen. Von Marc Moschettini
Erweiterte Marktzulassung
Das auf Afamelanotid basierende Medikament SCENESSE® aus dem Hause Clinuvel wird erfolgreich bei der Behandlung von erythropoetischer Protoporphyrie (EPP) eingesetzt, einer seltenen Krankheit, die schmerzhafte Lichtempfindlichkeit verursacht. Mit Health Canada prüft aktuell die Gesundheitsbehörde eines weiteren Landes die uneingeschränkte Marktzulassung. Bereits seit 2023 erfolgen in Kanada Behandlungen mit SCENESSE®, allerdings nur in einem kleinen, sogenannten „Special Access Program“ (SAP). Im Falle einer Zulassung, mit der in Q4/2025 gerechnet wird, könnten schätzungsweise 280 EPP-Patienten, für die es bis dato keine Behandlungsmöglichkeit gibt, im großen Maßstab von SCENESSE® profitieren. Neben Europa, den USA, Australien und Israel wäre das Medikament damit auch in Kanada flächendeckend erhältlich. Um die Behandlung von Patienten in ganz Nordamerika zu erleichtern, baut CLINUVEL sukzessive ein Netzwerk von geschulten und akkreditierten Spezialzentren auf. Die Gesamtzahl ist inzwischen auf 93 Zentren angestiegen, darunter vier in Kanada – anvisiert ist die Zielmarke von 120 Spezialzentren in Nordamerika, die noch in 2025 erreicht werden sollen.
Am 2. Juni 2025 findet in Frankfurt a.M. die 4. Summer Lounge Mitarbeiterbeteiligung statt. Alle Informationen zur Veranstaltung finden Sie hier. Zur Veranstaltung wird das GoingPublic-Special „Mitarbeiterbeteiligung“ erscheinen.
Einsatzgebiet Vitiligo
Auch bei den Bemühungen das Medikament als Plattformtechnologie für weitere Anwendungsgebiete, allen voran Vitiligo (Weißfleckenkrankheit), in Position zu bringen, gibt es Erfolge zu vermelden. Anfang Mai 2025 gab Clinuvel bekannt, dass man das Rekrutierungsziel für die Phase-III-Studie (CUV105) zu SCENESSE® mit über 200 Patienten erreicht habe. Die ersten Ergebnisse der Studie, die in 37 Studienzentren auf drei Kontinenten durchgeführt wird, werden in der zweiten Hälfte des Jahres 2026 erwartet. „Die ersten klinischen Beobachtungen der systemischen Lösung sind ermutigend, und wir werden nun die Diskussion über die Zulassung in Europa, Afrika und Nordamerika fortsetzen, und zwar in Erwartung von CUV107, einer zweiten großen Studie zur Bewertung der Behandlungseffekte von SCENESSE® bei Vitiligo“, legt Dr. Emilie Rodenburger, Director, Global Clinical Affairs bei CLINUVEL die weitere Marschrichtung fest. Gleichwohl ist die Rekrutierung der Vitiligo-Studie CUV105 mit hohen Kosten verbunden. Insgesamt sind die Ausgaben für klinische und nicht-klinische Entwicklung auf 2,8 Millionen AUD (ca. 1,6 Millionen EUR) gestiegen, was einem Anstieg von über 270 Prozent gegenüber dem Vorjahr entspricht. Zudem wird erwartet, dass die Kosten für klinische Studien auch künftig steigen werden, wenn die Patienten die Vitiligo-Studien (CUV105 und CUV107) sowie weitere Testreihen durchlaufen.
Kontinuität bleibt bestehen
Mitte März 2025 gab Clinuvel bekannt, dass CEO Dr. Wolgen sich – akut erkrankt – vom Tagesgeschäft zurückziehen müsse. Interimsmäßig wurde Chief Operations Officer (COO) Lachlan Hay vom Board of Directors zum amtierenden CEO unter der Leitung von Dr. Wolgen ernannt. Das bestehende Führungsteam des Unternehmens werde die täglichen Aufgaben von Dr. Wolgen für bis zu drei Monate übernehmen und so für eine kontinuierliche Unternehmensführung in dieser wichtigen Phase der Neuausrichtung des Unternehmens sorgen, hieß es von Seiten des Unternehmens. Parallel sei man auf der Suche nach einem neuen CEO, wobei „eine amerikanische Führungspersönlichkeit“ bevorzugt werde.
Photokosmetik als zweites Standbein
Die flächendeckende Markteinführung von CYACÊLLE Radiant, einem ultrawirksamen Sonnenschutz gegen UVA, UVB und 80 Prozent des blauen Lichts – ist für das Spätjahr 2025 geplant. Damit beschreitet Clinuvel einen wichtigen Schritt, „um eine weitere (Nicht-Rx-) Einnahmequelle zu schaffen“. Die Schwerpunkte der strategischen Ausrichtung der PhotoCosmetics liegen auf den Bereichen „Protect“, „Preserve“ und „Bronze“, so dass sukzessive Erweiterungen hinsichtlich Breite und Tiefe des Sortiments angedacht sind. Als nächstes sind die ersten Melanocortin-Produkte geplant, allen voran CLINUVEL Preserve-Assisted DNA Repair. Die medienwirksame Einführung wird mit exklusiven Events in den Alpen und anderen Hotspots in den Bergen erfolgen. Im Hochsommer 2026 soll dann in einem weiteren Schritt das Bräunungsprodukt Bronze-Melanogenesis von CLINUVEL lanciert werden.
„Wir denken nicht in Jahren, sondern in Jahrzehnten.“
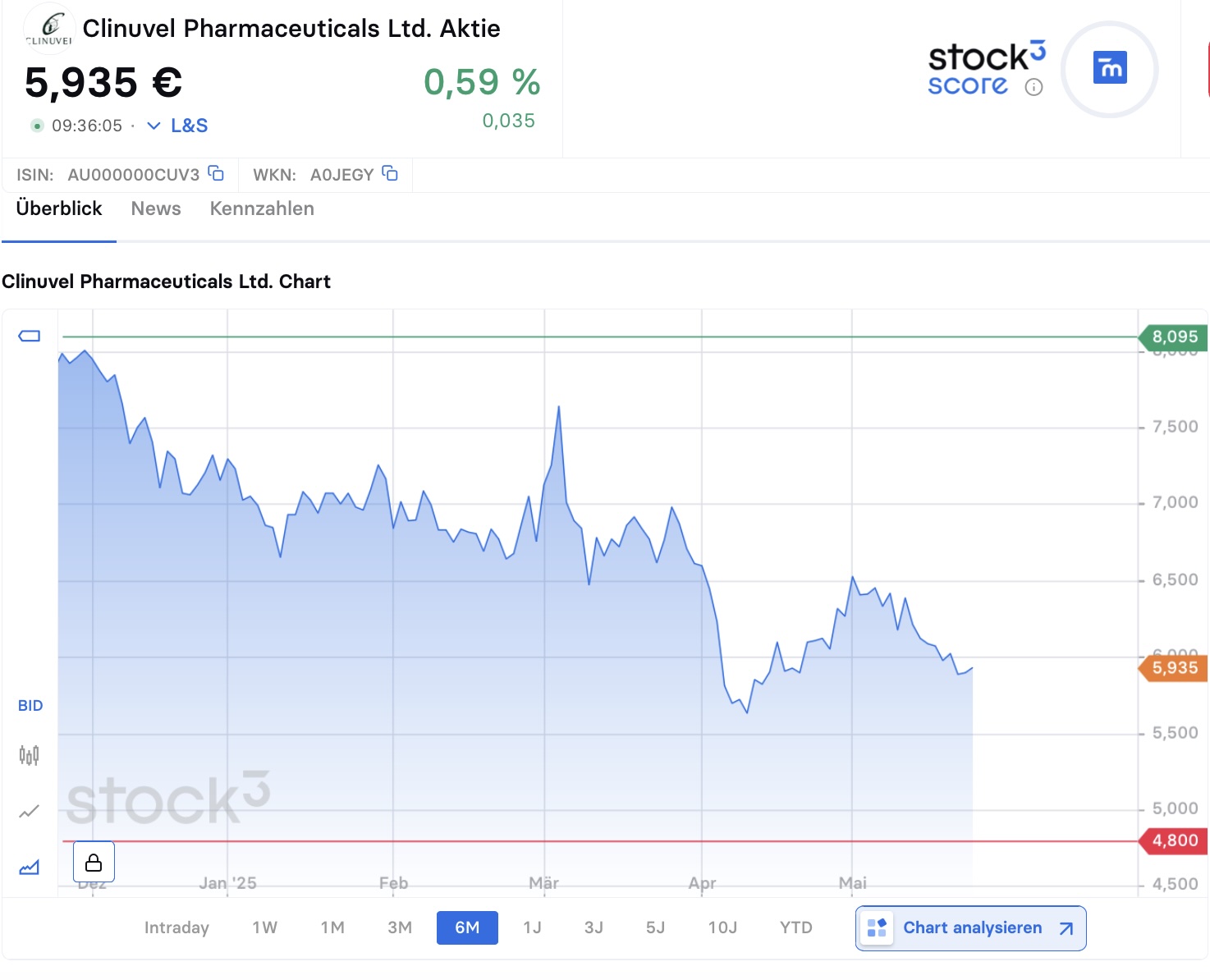
Kursentwicklung hinkt hinterher
Wenig Grund zur Freude liefert indes der Aktienkurs. Aktuell notiert das Papier unter 11 AUD (ca. 6 EUR) und konnte damit weder von guten Zahlen noch von erreichten Meilensteinen der Phase-III-Studie profitieren. Am Markt scheint der Fokus verstärkt auf die Kostenseite gerichtet zu sein, die zwar ohne Fremdmittel bestritten werden können, aber dennoch in naher Zukunft anfallen. Da mit endgültigen Ergebnissen auf Wachstumstreiber Vitiligo nicht vor 2026 gerechnet wird, scheint zudem die unmittelbare Kursfantasie begrenzt. Gleichwohl kann unabhängig davon eine erfolgreiche Umsatzausweitung in Q1/ 2025 verkündet werden, die sowohl auf die Zunahme der Patientenzahl, dem Anstieg der Behandlungsdosen pro Patienten und der gewachsenen Zahl der verschreibenden Ärzte zurückzuführen ist.
Fazit
Die Erkrankung von CEO Dr. Wolgen und die damit verbundene Unsicherheit ist sicherlich einer der Gründe, dass der Aktienkurs hinter den Erwartungen zurückblieb. Auch wenn prinzipiell Geduld gefragt ist, da bedeutende Meilensteine hinsichtlich Vitiligo-Zulassung wohl erst in 2026 anstehen, gibt es aber auch Entwicklungen, die kurzfristig für Kursphantasie sorgen könnten. So könnte beispielsweise eine anstehende Entscheidung der Europäischen Arzneimittel-Agentur (EMA) über eine Zulassungsänderung als nächster Wachstumskatalysator fungieren. CLINUVEL befindet sich aktuell in einem fortgeschrittenen Stadium der Gespräche mit der EMA, um die empfohlene maximale Anzahl von Dosen pro Jahr von SCENESSE® für erwachsene Patienten mit EPP von derzeit vier auf bis zu sechs subkutanen Dosen pro Jahr zu erhöhen.
Aufgrund dieser Steigerung von bis zu 50 Prozent würde sich der zusätzliche Umsatz auf einen mittleren zweistelligen Millionenbetrag pro Jahr erhöhen. Spätestens dann würde wohl auch der Kurs wieder gen Norden zeigen, auch wenn man bei Clinuvel das große Ganze im Blick hat: „Wir denken nicht in Jahren, sondern in Jahrzehnten, denn so lange dauert es eine robuste Technologieplattform auszubauen und ein Unternehmen zu etablieren, das seine Innovationen direkt für Krankenhäuser entwickelt, vermarktet und vertreibt. Wir verstehen uns als eine Weglege-Aktie, die drei Generationen begeistern wird“, so das Unternehmen in einem Statement.
Autor/Autorin

Marc Moschettini
Marc Moschettini ist Mitglied des GoingPublic-Autoren-Teams. Er studierte BWL an der LMU München/ ESC Lyon und ist seit über 15 Jahren als freier Wirtschafts- und Finanzjournalist tätig. In den Bereichen Aktien, Fonds und Derivate publiziert er im deutschsprachigen Raum u.a. für Fachmagazine, Onlineplattformen und Newsletter.