Bildnachweis: InflaRx, stock3.com, Kristina Blokhin – stock.adobe.com.
Die seit Ende 2017 an der Nasdaq gelistete Biotechfirma aus Jena bleibt bei den Einnahmen aus ihrem ersten zugelassenen Medikament bislang deutlich unter den Erwartungen. Umso mehr setzt InflaRx (WKN: A2H7A5 ISIN: NL0012661870) in diesem Jahr auf kurstreibende Impulse durch die klinischen Resultate von zwei weiteren Hoffnungsträgern, die in Entzündungskrankheiten mit hohem medizinischem Bedarf den kommerziellen Durchbruch schaffen sollen. Gelingt das, steht das aktuell bei 70 Mio. EUR Marktkapitalisierung stehende Unternehmen vor einer Neubewertung. Von Stefan Riedel
Für InflaRx wird 2025 zu einem Schlüsseljahr. Die klinischen Ergebnisse von zwei Produkten aus der Pipeline des Jenaer Biotechunternehmens könnten sich dabei als die zwei größten Kurstreiber für die Aktie erweisen. Gohibic, das erste zugelassene Produkt von InflaRx, hat dagegen bislang die Umsatzerwartungen enttäuscht. Ganze 200.000 EUR Umsatz spülte das zur Behandlung von schwer erkrankten und künstlich beatmeten COVID-19-Patienten in den USA zugelassene Präparat 2024 in die Kasse. Demgegenüber stehen 2,8 Mio. EUR Umsatzkosten für das eigene Vertriebsteam, die in der Bilanz verbucht wurden. Der Konzernverlust vergrößerte sich gegenüber 2023 von 42,7 auf 46,2 Mio. EUR oder 0,87 EUR je Aktie.
Gohibic und der Hoffnungsschimmer Europa
Ob und wie InflaRx mit Gohibic in Europa abschneiden wird, muss sich noch zeigen. Im Januar 2025 erhielt Gohibic die EU-weite Zulassung zur Behandlung des durch das SARS-CoV-2-Virus induzierten akuten Atemnotsyndroms. Welche Marketingstrategie InflaRx einschlagen wird, ist noch offen.

„Wir prüfen derzeit verschiedene Optionen für kommerzielle Partnerschaften und Vertriebswege in der EU. Wichtig ist, dass wir nicht erwarten, dass sich dieser Ansatz wesentlich negativ auf unsere Cash-Burn-Rate auswirken wird“, erläutert Vorstandschef Niels Riedemann gegenüber Plattform Life Sciences. Um das bisherige Verlustgeschäft im eigenen Marketing abzufedern, muss InflarX eine Verpartnerung zu halbwegs attraktiven Konditionen gelingen.
Aber: zwei Pipelinekandidaten haben das Zeug zum Kurstreiber
Umso mehr richtet sich der Blick der Investoren in diesem Jahr auf die erwarteten klinischen Resultate von zwei Pipelinekandidaten in insgesamt drei Indikationen. InflaRx startete im November 2024 mit der Rekrutierung der ersten 30 Patienten für die zulassungsrelevante Phase-3-Studie von Vilobelimab zur Behandlung von Pyoderma Gangrenosum (PG), einer seltenen und schmerzhaften Hauterkrankung mit offenen Geschwüren. Eine Zwischenanalyse aus dieser Studie wird bis Ende Mai 2025 erwartet. Diese Analyse entscheidet den weiteren Weg: Entweder die Studie wird fortgesetzt mit einer Patientenzahl, die in dieser Interimsanalyse festgelegt wird und zwischen 50 bis 100 Patienten liegen soll, oder sie wird aufgrund von fehlenden Wirksamkeitssignalen gestoppt.
Weil diese Krankheit bis dato kaum behandelbar ist, wäre das Marktpotenzial enorm.
InflaRx, so lässt Riedemann durchblicken, könnte sich auch bei PG vorstellen, den US-Markt mit eigenem Vertriebsteam anzugehen. Was im Umkehrschluss weitere Investitionen in die Vertriebsstrukturen bedeutet. Das Unternehmen zieht aber auch weltweit Partnerschaften in Betracht.
Es folgen in den Sommermonaten die ersten Wirksamkeitsresultate für INF904 in einer Phase-2a-Studie in der Behandlung von Chronischer spontaner Urtikaria (CSU) und Hidradenitis Suppurativa (HS), zwei chronischen Hauterkrankungen, die im Fall von HS durch Autoimmunreaktionen ausgelöst wird. Nach Angaben von InflarX eröffnen sich in beiden Indikationen kommerzielle Opportunitäten mit einem jährlichen Umsatzpotenzial von jeweils mehr als eine Mrd. USD. Strategisch hält sich InflarX laut Riedemann alle Optionen offen: „Wenn die Phase-2a-Daten dies unterstützen, planen wir, INF904 in einer längerfristig angelegten Phase-2b-Studie in den Indikationen HS aber auch CSU zu untersuchen. Gleichzeitig sind wir offen für Kollaborationen, sollten diese für unsere Anteilseigner einen attraktiveren Weg darstellen.“
Alle Therapien hemmen gezielt einen Teil des Komplementsystems, das zum angeborenen Immunsystem gehört. Dieser spielt eine zentrale Rolle bei akuten und chronischen Entzündungen. Durch die Ausschüttung von spezifischen Enzymen bekämpfen die neutrophilen Granylozyten bakterielle und virale Entzündungsherde.
Kapitalerhöhung sichert PG-Studie
Finanziell ist InflaRx bis ins Jahr 2027 durchfinanziert. Den entscheidenden Schritt dafür war die Kapitalerhöhung vom Februar. Dem Bruttoemissionserlös von 28,7 Mio. EUR zugrunde lag die Ausgabe von 8,25 Mio. neuen Aktien in einem öffentlichen Angebot zu einem Preis von 2,00 USD je Aktie. „Unser Ziel mit dieser Kapitalerhöhung war klar: Unsere finanzielle Laufzeit bis 2027 nachhaltig zu verlängern und den Datenerhalt aus der PG-Studie finanziell abzusichern“, so Riedemann zum Grund für die Kapitalmaßnahme.
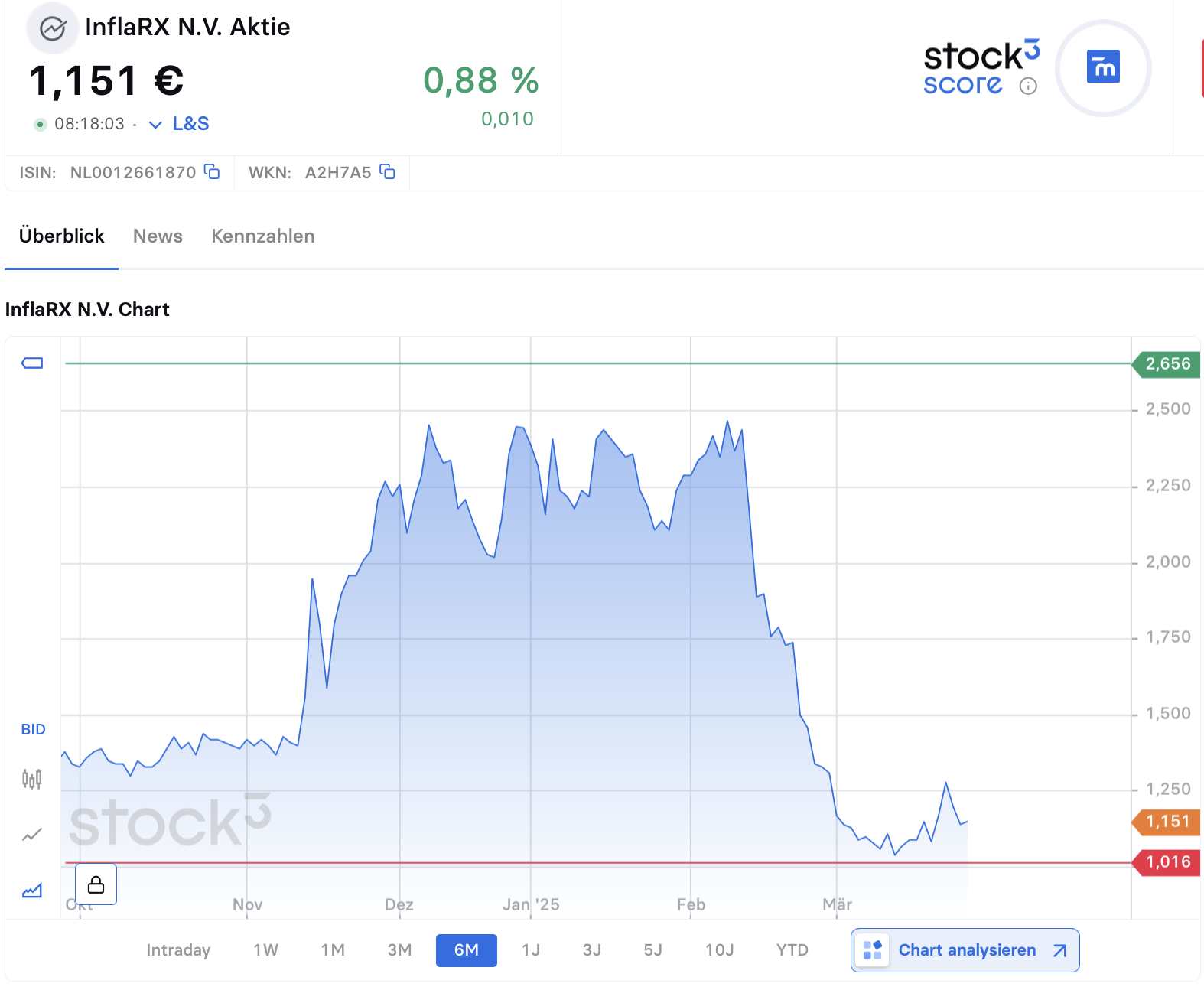
In der Summe verfügt InflarX aktuell über rund 80 Mio. EUR an Cashreserven, was in etwa dem aktuellen Börsenwert entspricht. Der Aktienkurs geriet als Reaktion auf den Finanzierungsschritt negativ: In der Spitze halbierte sich der Börsenwert. Im März ist der Aktienkurs zu einer charttechnischen Bodenbildung übergegangen. Entscheidend für eine Trendwende zu einem neuen Aufschwung wird der Nachrichtenfluss in den kommenden Monaten. Bis dahin zeichnen sich keine größeren kursbewegenden Ereignisse ab.
Autor/Autorin

Stefan Riedel
Stefan Riedel ist in den internationalen Finanzmärkten unterwegs. Seit 20 Jahren schreibt der passionierte Börsianer für die Plattformen und Publikationen von GoingPublic Media, unter anderem GoingPublic und die Plattform Life Sciences.