Bildnachweis: © Formycon AG.
Steigende Marktanteile mit allen Produkten, ein deutlich verbessertes Marktumfeld in den USA und erste Vermarktungspartnerschaften für ein Krebs-Biosimilar – Dr. Stefan Glombitza erläutert im Gespräch, wie der Biosimilarspezialist Formycon ab 2026 nachhaltig profitabel arbeiten will.
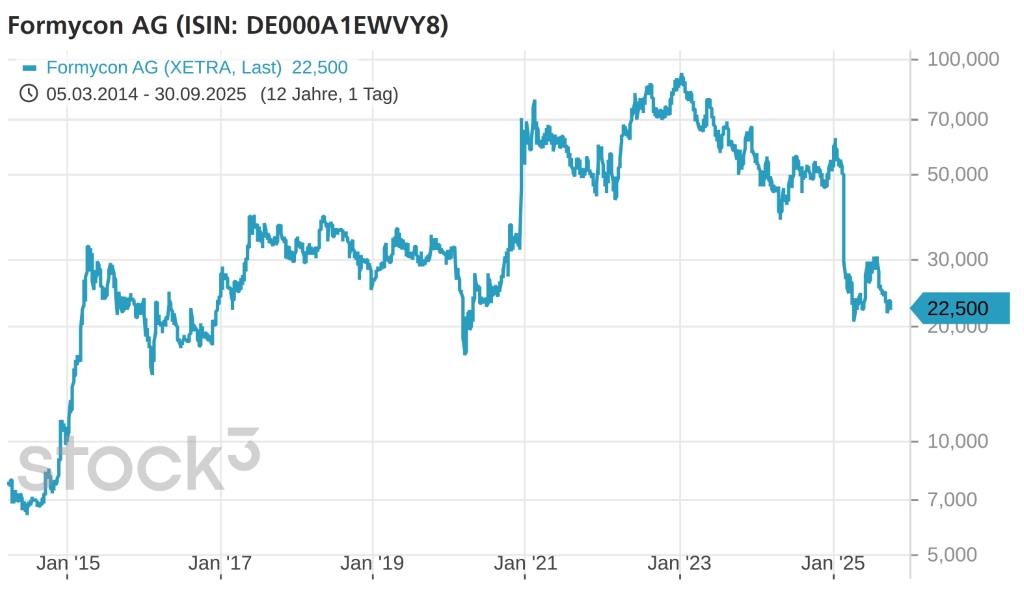
Plattform Life Sciences: Herr Dr. Glombitza, ein dichter Nachrichtenfluss, aber zugleich ein heftiger Kurseinbruch – 2025 war für Formycon bislang ein schwieriges Börsenjahr. Welche Entwicklung im operativen Geschäft erwarten Sie bis zum Jahresende?
Dr. Glombitza: Die vielen positiven Ereignisse im operativen Geschäft und der Aktienkurs haben sich 2025 nicht unmittelbar parallel entwickelt. Im ersten Halbjahr konnten wir mit neuen Partnerschaften zur Kommerzialisierung und Fortschritten in unserer Entwicklungspipeline starke Impulse setzen. Zugleich resultierte die im Februar angekündigte Wertberichtigung in einer deutlichen Kursreaktion, von der sich die Aktie noch nicht erholt hat. Bis zum Jahresende stehen noch weitere wichtige Meilensteine an, darunter die europäische Einführung der Fertigspritze für unser Lucentis-Biosimilar, zusätzliche Fortschritte und Verpartnerungen unserer Pipelinekandidaten sowie öffentliche Informationen zu unserem Pipelineprojekt FYB208.
FYB206, das am weitesten fortgeschrittene Pipelineprodukt, ist ein Biosimilar für das weltweit meistverkaufte Krebsmedikament, KEYTRUDA, das ab 2029 in den USA und 2030 in Europa seinen Patentschutz verliert. Was will Formycon hier noch 2025 erreichen?
Bereits im Juli haben wir die Rekrutierung aller Patienten für unsere Phase-I-Studie abgeschlossen und erwarten im ersten Quartal 2026 die Ergebnisse. Nach dem positiven Phase-III-Waiver der FDA für FYB206 – also die Mitteilung, dass die bereits vorliegenden klinischen Daten aus der laufenden Phase-III-Studie für den Zulassungsantrag ausreichen – ist die einzige im Rahmen der klinischen Entwicklung notwendige Studie bereits sehr weit fortgeschritten. Wir haben uns damit einen guten Zeitvorsprung gegenüber den Mitbewerbern erarbeitet und sehen ein entsprechendes Momentum für eine frühe Verpartnerung. Erste Vermarktungspartner für FYB206 wollen wir noch 2025 präsentieren. Die damit verbundenen Down Payments für den Abschluss von Lizenzdeals gegen Ende des Jahres stellen auch eine Komponente unserer Umsatzerlöse für 2025 dar.
Welche Qualitätsmerkmale müssen Marketingpartner für Sie mitbringen?
Wie bei unseren drei bislang zugelassenen Produkten streben wir Partnerschaften mit regionalen Champions an. Für die optimale Kommerzialisierung müssen die potenziellen FYB206-Lizenzpartner die Vermarktungsstrukturen innerhalb der Onkologie und den einzelnen Märkten sehr gut kennen sowie effiziente und schlagkräftige Vertriebsstrukturen besitzen. Ein exzellentes Netzwerk innerhalb der Zielmärkte ist dabei der Hebel zum Erfolg.
Größere Patientengruppen in den USA mit Biosimilars zu adressieren, bleibt im aktuellen Marktumfeld eine der größten Herausforderungen. Wie geht Formycon strategisch vor?
Verglichen mit Europa ist der US-Biosimilarmarkt, der erst 2016 startete, ein junges Segment, aber mit dynamischer Entwicklung. Regulatorisch sind positive Bewegungen erkennbar, etwa die zunehmende Bereitschaft der FDA, in bestimmten Fällen auf Phase-III-Studien zu verzichten. Dies unterstützt die weitere Öffnung des Biosimilar-Markts und das Ziel, Arzneimittelkosten nachhaltig zu senken. Im Medical-Benefit-Bereich, etwa in Ophthalmologie und Onkologie, erreichen Biosimilars bereits Marktanteile von 50% bis 80%. Im Pharmacy-Benefit-Segment gestaltet sich der Zugang durch komplexe Einkaufsstrukturen über sogenannte Pharmacy Benefit Manager (PBMs) deutlich schwieriger. Dennoch wächst auch hier die Nutzung Schritt für Schritt und unser Partner treibt die Vermarktung aktiv voran.
Nach welchem Risiko-Rendite-Profil werden nach Ihrer Wahrnehmung reine Biosimilarspezialisten wie Formycon an den Finanzmärkten bewertet – insbesondere im Vergleich zu Pharma- und Biotechaktien?
Biosimilarunternehmen werden vom Kapitalmarkt häufig noch nach dem Risikoprofil klassischer Biotechs bewertet, obwohl die klinische Erfolgswahrscheinlichkeit der Biosimilars im Vergleich zu innovativen Produkten schon in frühen Entwicklungsphasen bei über 70% liegt. Herausfordernder ist es, die Entwicklung von Markt, Preisen und Wettbewerb im Biosimilarsegment zuverlässig einzuschätzen. Der Tenor aus unseren Gesprächen mit Investoren und Analysten ist aber: Biosimilars sind ein Wachstumssegment. Unser Fokus liegt daher darauf, die Wahrnehmung am Kapitalmarkt gezielt zu schärfen, dass sich Formycon in der Transformation zu einem nachhaltig profitablen Unternehmen befindet.
Anders als zuletzt die Formycon-Aktie wurde an den Finanzmärkten die Anleihe mit vierjähriger Laufzeit angenommen, die Formycon im Juni zu einem Gesamtvolumen von 70 Mio. EUR platziert hat.
Mit der Platzierung der Anleihe sind wir sehr zufrieden. Die Aufstockung der ursprünglich antizipierten 50 Mio. auf 70 Mio. EUR zeigt das große Interesse an diesem Finanzierungsinstrument. Die Platzierung dieser Anleihe ist ein Beleg für unser funktionierendes und belastbares Geschäftsmodell. Investoren zeichnen in der Regel Anleihen profitabler Firmen. Daher werten wir das Investoreninteresse als Bestätigung dafür, dass unser Ziel – spätestens 2027 auf EBITDA-Basis profitabel zu sein und die Anleihe bis 2029 vollständig zurückzuzahlen – am Kapitalmarkt als glaubwürdig eingeschätzt wird.
Haben neue Investorengruppen die Anleihe gezeichnet?
Tatsächlich haben internationale Investoren die Anleihe gezeichnet. Der größte Teil davon kam aus den USA, aber auch aus Skandinavien.
Unter welchen Voraussetzungen eignet sich nach Ihrer Einschätzung das Investmentvehikel Anleihe für europäische Unternehmen aus der Life-Sciences-Industrie?
Ein belastbares Geschäftsmodell muss skalierbare Produkte und stabile Cashflows ermöglichen. Außerdem muss die Gewinnzone zumindest in Reichweite liegen. Trifft dies alles zu, überzeugt das Investoren davon, dass eine Rückzahlung des Kredits realistisch und planbar ist.
Was ist auf Sicht der nächsten 24 Monate entscheidend, um auf dem Weg zu einem profitablen Produktunternehmen voranzuschreiten?
Kurzfristig liegt der Fokus auf der weiter steigenden Marktdurchdringung von FYB202 in den USA und der EU. Besonders im US-Markt beobachten wir seit Jahresbeginn eine spürbare Veränderung der Vertragsabschlüsse. Parallel dazu steht der Relaunch von FYB201 im US-Markt bevor, ergänzt durch die Einführung der anwendungsfreundlichen Fertigspritze in einzelnen europäischen Ländern. Für FYB203 rechnen wir mit ersten Markteinführungen, sobald die rechtliche Situation dies erlaubt. Ebenso streben wir erste Einnahmen über einzelne Lizenzverträge aus der Verpartnerung von FYB206 an. Die Diversifikation unserer Absatzmärkte schreitet ebenfalls voran, etwa mit FYB201 in Afrika und Lateinamerika. Liefern wir in den beschriebenen Bereichen wie geplant, sehen wir gute Voraussetzungen, ab 2026 nachhaltig profitabel zu wirtschaften.
Wie hat sich parallel zur Entwicklung im operativen Geschäft die Investorenbasis entwickelt?
In geografischer Hinsicht ist der Anteil der US-Investoren gestiegen. Das Thema Biosimilars kommt in den USA immer mehr an, und zwar sowohl bei den Generalisten als auch bei den Healthcarespezialisten. Im deutschsprachigen Raum interessieren sich vor allem die Generalisten unter den institutionellen Investoren für unsere Equity Story. Das hängt auch damit zusammen, dass bereits etliche Biosimilars in Europa auf dem Markt sind und sich bewährt haben. Zugleich haben das Uplisting in den Prime Standard und die Aufnahme in den SDAX die Visibilität der Aktie erhöht. Dazu kommt das allgemein gestiegene Interesse der US-Investoren an europäischen Aktien. Dieses Momentum wollen wir nutzen.
Erwarten Sie, dass sich an den Kapitalmärkten das Börsenklima für Gesundheitsaktien aus dem Gesundheitssektor in naher Zukunft wieder aufhellen wird?
Unser Eindruck von den Konferenzen der letzten Monate ist, dass sich die Stimmung im Vergleich zum Vorjahr wieder verbessert. Natürlich können wir uns externen Faktoren wie der US-Handelspolitik nicht entziehen. Die aktuellen preisregulatorischen Maßnahmen zielen allerdings aus unserer Sicht eindeutig auf die hochpreisigen Referenzarzneimittel ab. Biosimilars sind für die Gesundheitsbudgets ein wichtiger Teil der Lösung und stehen in den USA – vergleichbar mit der EU – bereits für kompetitive Preise. Entscheidend für uns ist, durch das konsequente Erreichen unserer operativen Ziele das Vertrauen der Finanzmärkte weiter zu festigen und nachhaltig auszubauen.
Herr Dr. Glombitza, vielen Dank für das Gespräch.
Das Interview führte Stefan Riedel.
Zum Interviewpartner

Autor/Autorin

Stefan Riedel
Stefan Riedel ist in den internationalen Finanzmärkten unterwegs. Seit 20 Jahren schreibt der passionierte Börsianer für die Plattformen und Publikationen von GoingPublic Media, unter anderem GoingPublic und die Plattform Life Sciences.