Bildnachweis: airdone – stock.adobe.com, AC Immune.
Parkinson betrifft weltweit mehr als 6 Millionen Menschen. In den meisten Fällen ist die Ursache der Erkrankung unbekannt, aber Wissenschaftler arbeiten hart daran, die Auslöser und die Kaskade der zellulären Veränderungen im Gehirn zu verstehen. Ein besseres Verständnis könnte den Forschern helfen, Behandlungen zu entwickeln, die die Krankheit aufhalten oder sogar verhindern. Prof. Andrea Pfeifer ist Gründerin und CEO von AC Immune, einem Biotech-Unternehmen, das sich auf die Entwicklung von Diagnostika und Therapien für neurodegenerative Erkrankungen spezialisiert hat. In ihrem Beitrag aus Anlass des „Parkinson Awareness Monat“ April erörtert sie, wie die Gesundheitsbranche diese verheerenden Krankheiten behandeln und schließlich verhindern will.
Die biopharmazeutische Industrie arbeitet an innovativen und wirksameren Lösungen für die enormen und dringenden Herausforderungen der Gesundheitsversorgung im Zusammenhang mit neurodegenerativen Krankheiten. Neurodegenerative Erkrankungen, einschließlich der Parkinson-Krankheit (PD) und der Alzheimer-Krankheit (AD), sind zwar keine Infektionskrankheiten, können aber als eine stille Pandemie mit ständig wachsender Prävalenz beschrieben werden. Die zunehmende Inzidenz führt zu einer gesellschaftlichen und wirtschaftlichen Situation, die dringend angegangen werden muss.

Dank der Fortschritte auf dem Gebiet der genetischen und diagnostischen Biomarker ist es heute möglich, Menschen mit einem Risiko für neurodegenerative Erkrankungen 10-20 Jahre vor dem Auftreten von Krankheitssymptomen zu identifizieren, so dass eine Behandlung mit potenziell krankheitsverändernden Medikamenten viel früher möglich ist. Eine frühzeitige Identifizierung könnte eine Impfung ermöglichen und sie zum effizientesten und wünschenswertesten Weg machen, um neurodegenerative Erkrankungen langfristig zu verhindern und zu behandeln.
Wie könnte ein Impfstoff gegen Parkinson aussehen und warum könnte er die Behandlung neurodegenerativer Erkrankungen revolutionieren?
Neurodegenerative Erkrankungen weisen charakteristische Merkmale auf, die eine aktive Immunisierungsstrategie zu einem praktikablen und attraktiven Ansatz machen. Bestimmte fehlgefaltete Versionen von Proteinen – wie Amyloid beta (Abeta), Tau und Alpha-Synuclein (a-syn) – gelten als Hauptfaktoren der Neurodegeneration. Bei Morbus Parkinson bildet fehlgefaltetes a-syn Aggregate, die als Lewy-Körperchen bekannt sind. In ähnlicher Weise bilden Abeta und Tau bei Alzheimer fehlgefaltete Abeta-Plaques und Tau-Tangles.
Wissenschaftler erforschen seit längerem Impfstoffe, die auf diese Proteine abzielen und die Neurodegeneration behandeln sollen. Frühe Versuche verliefen allerdings enttäuschend. Der Grund hierfür könnte sein, dass sie sich nicht auf die fehlgefalteten oder pathologischen Formen der Proteine konzentrierten. Die Impfstofftechnologien machen Fortschritte, und neue gezielte Ansätze könnten das Fortschreiten der Krankheit verlangsamen.
Unter der Voraussetzung, dass Fortschritte in der Diagnostik eine frühere Erkennung ermöglichen, könnten Therapeutika, die fehlgefaltete Proteine beseitigen. Sie würden so eine Möglichkeit bieten, den mit dem Fortschreiten der Krankheit verbundenen motorischen Funktionsverlust zu verlangsamen, aber vielleicht auch das Auftreten von Symptomen zu verhindern. Da Impfstoffe das Immunsystem stimulieren um die Antikörper selbst zu produzieren, könnten diese weniger häufig verabreicht werden als extern produzierte monoklonale Antikörper (mAb) oder niedermolekulare Therapeutika. Dadurch wäre es auch für die Patienteneinfacher, die Behandlungspläne einzuhalten, und die Kosten könnten erheblich niedriger sein.
Werden diese Impfstoffe wirken?
Neue Impfstoffe, die auf die charakteristischen Proteinopathien neurodegenerativer Erkrankungen wie Morbus Parkinson oder Alzheimer abzielen, befinden sich in der Mitte der klinischen Entwicklung, was bedeutet, dass wir bald wissen werden, ob sie Vorteile bringen können. Die jüngsten Fortschritte bei den monoklonalen Antikörpern sind wegweisend. Klinische Versuche mit Forschungsantikörpern, die auf fehlgefaltete Proteine abzielen, haben kürzlich a-syn, Tau und Abeta als therapeutische Ziele bestätigt und vielversprechende Ergebnisse bei Parkinson und Alzheimer gezeigt.
| Vaccine | Target | Status | Entwickler |
| PD01/ACI 7104 | alpha-synuclein | Parkinson’s disease Phase II | AC Immune |
| UB-312 | alpha-synuclein | Parkinson’s disease Phase I | Vaxxinity |
| ABvac 40 | Amyloid | Alzheimer’s disease Phase II | Araclon Biotech |
| ACI-24 | Amyloid | Alzheimer’s disease Phase II; Alzheimer’s disease in Down’s Syndrome Phase Ib | AC Immune |
| UB-311 | Amyloid | Alzheimer’s disease Phase II | Vaxxinity |
| AADvac1 | Tau | Alzheimer’s disease Phase II; Progressive Nonfluent Aphasia Phase I | Axon Neuroscience |
| ACI-35.030 | Tau | Alzheimer’s disease Phase I/II | AC Immune, Janssen |
Quelle: AC Immune und clinicaltrials.gov
Da monoklonale Antikörper eng mit den Antikörpern verwandt sind, die unser Körper als Reaktion auf Impfstoffe bildet, liefern diese Ergebnisse auch den Beweis, dass eine Impfung funktionieren kann. Außerdem kann der Körper bei einer Impfung im Laufe der Zeit eine potenziell bessere Wirksamkeit entwickeln als bei monoklonalen Antikörpern, möglicherweise mit weniger Nebenwirkungen und weniger häufiger Verabreichung.
Derzeit werden mehrere Parkinson-Antikörper und Impfstoffe an Patienten getestet (s. Abb. 1). Der Impfstoff PD01/ACI-7104 zum Beispiel zeigte ermutigende Ergebnisse, die in The Lancet Neurology1 veröffentlicht wurden. Die Ergebnisse der Phase-I-Studie zeigten, dass der Impfstoff sicher und gut verträglich war und zu einer starken und durch Booster steigerungsfähigen Antikörperreaktion führte, die durch eine 50-prozentige Verringerung des pathologischen a-syn in der Gehirn-Rückenmarks-Flüssigkeit nachgewiesen werden konnte. Dieser Impfstoff soll noch in diesem Jahr in eine Phase-2-Studie aufgenommen werden, um die Wirksamkeit bei Patienten zu untersuchen.
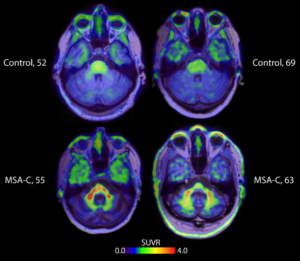
Darüber hinaus hat das Team von Dr. Oskar Hansson, Neurologe am Universitätskrankenhaus von Skåne und Professor für Neurologie an der Universität Lund, Schweden, letzten Monat auf dem AD/PD-Kongress zum ersten Mal nachgewiesen, dass es möglich ist, a-syn, das wichtigste Target bei Morbus Parkinson nachzuweisen. Mit einem PET-Tracer (ACI-12589) wurden bei einer Tomographie erstmals Live-Bilder des pathologischen Proteins im Gehirn von Patienten erzeugt (s. Abb. 2). Obwohl weitere Analysen erforderlich sind, könnten die Ergebnisse zur Entwicklung des ersten Diagnoseinstruments für Parkinson führen. Wichtig ist auch, dass die biopharmazeutische Industrie dadurch in die Lage versetzt werden könnte, die Wirkung von Therapien auf Patienten während klinischer Studien zu bewerten und die Entwicklung wirksamer neuer Behandlungen zu beschleunigen.
Zusammengenommen sind diese Ergebnisse sowie andere neue Daten äußerst ermutigend: Sie liefern einen echten Beweis für einen greifbaren Fortschritt, wie er seit Jahrzehnten nicht mehr zu beobachten war. Die neue Klasse von Impfstoffen, die sich in der Entwicklung befindet, hat nun ein geringeres Risikoprofil. Verbesserte Zulassungswege und die größere Menge an Daten, die mit Hilfe von Diagnoseinstrumenten zur Verfügung stehen, werden dazu führen, dass die Entwicklungsentscheidungen besser fundiert sind.
Große Chancen für die Gesundheitswirtschaft und für Investoren
Die Ergebnisse klinischer Studien sind wichtige Meilensteine, um neurodegenerative Erkrankungen mit Hilfe der Präzisionsmedizin zu adressieren. Hier gibt es einen gewaltigen medizinisch unterversorgten Markt. Und dieser Markt hat mit dem rasch wachsenden Anteil der über 65-Jährigen an der Bevölkerung einen wesentlichen Treiber.
Ziel der Präzisionsmedizin ist es, die Krankheitsursachen und -verläufe der einzelnen Patienten genauer zu diagnostizieren um schneller eine maßgeschneiderte Therapie bereitzustellen, was zu signifikanten Kostensenkungen führen kann. Die moderne Diagnostik, die auch genetische, molekulare und zelluläre Besonderheiten in die Therapieentscheidung einfließen lässt, ist dafür das Fundament. In der Krebsforschung hat die Präzisionsmedizin bemerkenswerte Fortschritte bewirkt. Die jahrzehntelange Arbeit in Hochschulen und Forschungslaboren hat und wird sich in der Entwicklung einer neuen Klasse von Medikamenten niedergeschlagen.
Die Fortschritte der personalisierten Medizin zwingt gleichzeitig Big Pharma dazu, ihr derzeitiges Geschäftsmodell zu überdenken. Das Blockbuster-Modell wird Platz machen für Arzneimitteltherapien, die auf den einzelnen Patienten zugeschnitten sind. Dies setzt voraus, dass die Medikamente schneller, wirksamer, sicherer und kostengünstiger entwickelt werden können. Im Zuge dieser Entwicklung werden so Biotech-Unternehmen, die Instrumente und Technologien beisteuern, die bessere Informationen, bessere Ergebnisse und niedrigere Kosten ermöglichen, immer wertvoller werden.
ZUR AUTORIN
Prof. Andrea Pfeifer ist CEO der AC Immune SA und hat das Unternehmen 2003 mitbegründet. Zuvor war sie Leiterin des Nestlé-Forschungszentrums in der Schweiz, wo sie die wissenschaftliche Entwicklung mehrerer innovativer Produkte vom Labor bis zur Marktreife leitete und den auf Biowissenschaften ausgerichteten Nestlé Venture Capital Fund mitbegründete. Sie ist Mitglied der CEOi-Initiative zur Alzheimer-Krankheit und der Davos Alzheimer’s Collaborative (DAC). Andrea Pfeifer hat an der Universität Würzburg in Toxikologie (Krebsforschung) promoviert und ist eingetragene Toxikologin und Pharmazeutin. Sie ist außerdem Honorarprofessorin an der Ecole Polytechnique Federale de Lausanne (EPFL).

