Bildnachweis: BillionPhotos.com – stock.adobe.com, stock3.com.
Der Antikörperkandidat Gotistobart von BioNTech (ISIN: US09075V1026) und OncoC4senkt in einem frühen Abschnitt einer globalen Phase-3-Studie das Sterberisiko bei fortgeschrittenem Lungenkrebs deutlich. Für die BioNTech-Aktie stellt sich damit die Frage, ob sich aus diesen klinischen Daten mittelfristig eine tragfähige Investmentstory außerhalb des COVID-19-Geschäfts ableiten lässt – oder ob der Markt die bestehenden Risiken weiterhin höher bewertet als die Chancen. Von Urs Moesenfechtel
Frühe Wirksamkeitssignale
In der ersten, noch nicht zulassungsrelevanten Phase der globalen Phase-3-Studie PRESERVE-003 wurde Gotistobart bei Patientinnen und Patienten mit metastasiertem Plattenepithelkarzinom der Lunge getestet – einer Form von Lungenkrebs, die nach einer PD-(L)1-Therapie und einer platinbasierten Chemotherapie häufig weiter fortschreitet. Für diese schwer zu behandelnde Gruppe gibt es nur wenige wirksame Standardoptionen, und die Prognose ist meist ungünstig. In diesem Studienabschnitt erhielten 45 Patientinnen und Patienten Gotistobart als alleinige Therapie; 42 Personen wurden mit dem Chemotherapeutikum Docetaxel behandelt (für die Sicherheitsbewertung lagen Daten von 41 Personen vor).
Überlebensrate verdoppelt
Zum Stichtag 8. August 2025 lagen Daten mit einer medianen Nachbeobachtungszeit von 14,5 Monaten vor. In diesem Zeitraum zeigte Gotistobart deutliche Vorteile: 63,1 Prozent der Behandelten waren nach zwölf Monaten noch am Leben, unter Docetaxel waren es 30,3 Prozent. Das mediane Gesamtüberleben im Chemotherapiearm lag bei 10 Monaten, während es unter Gotistobart zum Auswertungszeitpunkt noch nicht erreicht war. Dies entspricht einer Reduktion des Sterberisikos um 54 Prozent. Schwerwiegende Nebenwirkungen traten in beiden Gruppen in vergleichbarer Häufigkeit auf. Da diese Ergebnisse aus einem frühen, nicht-zulassungsrelevanten Studienabschnitt mit begrenzter Patientenzahl stammen, erlauben sie nur eine eingeschränkte Aussagekraft für die gesamte Zielpopulation. PRESERVE-003 ist zweistufig aufgebaut: Der nun ausgewertete Abschnitt dient der Dosisbestätigung. In der anschließenden, zulassungsrelevanten Hauptphase sollen nach aktuellem Studiendesign rund 500 Patientinnen und Patienten eingeschlossen werden. Primärer Endpunkt ist das Gesamtüberleben. Gotistobart verfügt über einen Fast-Track-Status der FDA sowie eine Breakthrough-Therapy-Designation der chinesischen NMPA. Parallel dazu laufen weitere PRESERVE-Programme in anderen Tumorindikationen sowie eine Kombinationserprobung mit BNT116.
Marktreaktion neutral
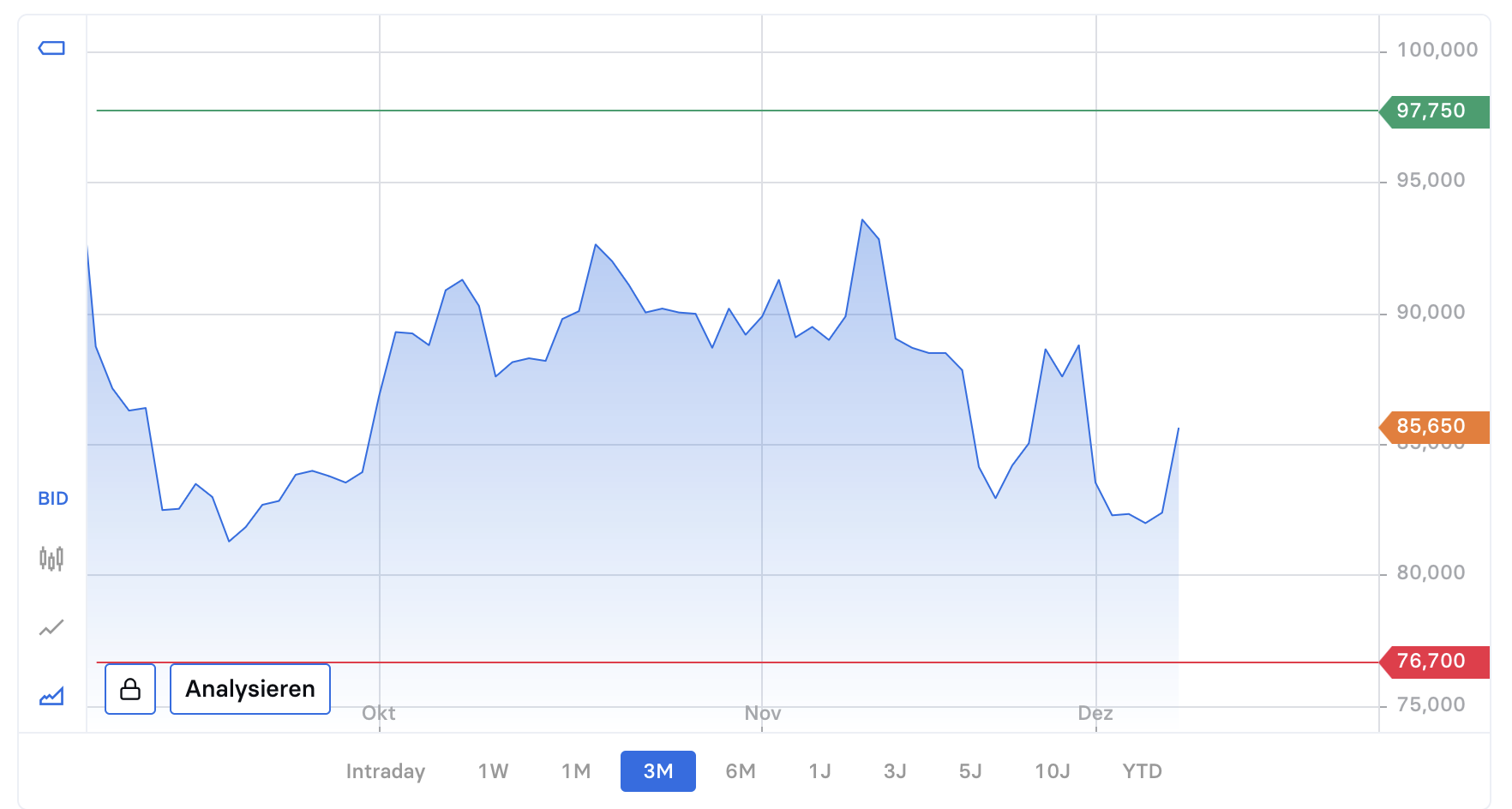
Zum 8. Dezember 2025 notiert die BioNTech-ADR bei 96,25 USD, die Marktkapitalisierung liegt derzeit bei 23,14 Mrd. USD. Damit bewegt sich der Kurs weiterhin unter dem 52-Wochen-Hoch von 122,80 USD. Das aktuelle Kurs-Umsatz-Verhältnis von 6,3 liegt nahe am Branchenschnitt von 6,6, was auf eine neutrale Bewertung hindeutet. Operativ meldete BioNTech im zurückliegenden Quartal einen Verlust von 0,14 USD je Aktie bei Umsätzen von 1,78 Mrd. USD. Die vorliegenden Gotistobart-Daten reduzieren zwar einen Teil des klinischen Risikos, stammen jedoch aus einem nicht-zulassungsrelevanten Studienteil – ein Grund für die weiterhin vorsichtige Einordnung des Marktes.
Ob und wie stark sich die neuen Studiendaten im Kurs widerspiegeln, dürfte sich im Verlauf dieser Woche zeigen. Die Ergebnisse machen deutlich, dass Gotistobart grundsätzlich wirken kann. Offen bleibt jedoch, ob sich der beobachtete Effekt im großen, zulassungsrelevanten Studienabschnitt bestätigt, wie stabil sich das Sicherheitsprofil über längere Behandlungszeiträume zeigt und welchen Platz das Medikament im Vergleich zu bestehenden Therapien einnehmen könnte. Da diese Punkte ungeklärt sind, löst das Studienergebnis noch keinen starken Kursimpuls aus, sondern führt eher zu einer vorsichtigen Anpassung der Erwartungen.
Autor/Autorin
Urs Moesenfechtel, M.A., ist Redaktionsleiter der Plattform Life Sciences und gehört zum Redaktionsteam der Kapitalmarkt-Plattform GoingPublic (GoingPublic, HV Magazin, www.goingpublic.de). Urs beschäftigt sich seit vielen Jahren mit den Themenfeldern Biotechnologie und Bioökonomie und war u.a. bereits als Wissenschaftsredakteur für mehrere Forschungseinrichtungen tätig.







