Krebs ist die medizinische Herausforderung unserer Zeit: Jeder Zweite erkrankt daran, jeder Vierte erliegt der Krankheit. Fakt ist aber auch: Seit rund dreißig Jahren geht die Krebssterblichkeit kontinuierlich zurück. Allein seit 1999 sind die Sterberaten um rund 20% gesunken. Verstärkte präventive Maßnahmen und eine verbesserte Früherkennung tragen erheblich dazu bei, vor allem aber auch der Medizineffekt: das Zusammenwirken von Diagnostik, Arzneimitteln und ärztlicher Behandlung. Und immer mehr vielversprechende Forschungsergebnisse und neuartige Arzneimittel der vergangenen Jahre kommen beim Patienten an. Bei einigen Krebserkrankungen haben sie das Blatt bereits gewendet, ermöglichen mehr und mehr Patienten Langzeitüberleben – selbst mit fortgeschrittenen Krebserkrankungen. In einigen Fällen sprechen wir sogar von Heilung. Von Prof. Dr. Hagen Pfundner
Wir wissen heute so viel wie noch nie über die Entstehung, das Fortschreiten und die Aggressivität von Krebs. Damit einher geht auch ein radikales Umdenken: Wir verstehen Krebs nicht mehr als eine Krankheit der Organe, sondern als Krankheit der Gene. Denn Brustkrebs ist nicht gleich Brustkrebs und Darmkrebs nicht gleich Darmkrebs. Deshalb wäre es auch fatal, Patienten anhand dieser Einteilung zu therapieren. Vielmehr entscheiden individuelle genetische Veränderungen darüber, ob eine Behandlung Erfolg haben wird oder nicht. In der Onkologie lassen sich diese genetischen Veränderungen in vier Buchstaben zusammenfassen: ACGT. Schier endlos reihen sie sich in jeder Zelle unseres Körpers in vermeintlich zufälliger Reihenfolge aneinander und bilden so unser Erbgut. Im Normalfall arbeiten die fast 40 Billionen Zellen unseres Körpers wohlkontrolliert und als Einheit zusammen. Zellteilung, Wachstum, Zelltod – alles wird streng und präzise gesteuert. Läuft dabei etwas schief, kommt es zu Mutationen. Unsere Zellen sind dann bestrebt, diese Fehler zu beseitigen. Gelingt das nicht, leitet die betroffene Zelle den programmierten Zelltod, die Apoptose, ein, um Schaden vom gesamten Organismus abzuwenden. Ist dies nicht möglich, steht zu guter Letzt unser Immunsystem bereit, um auffällige Zellen zu beseitigen. Versagen diese Mechanismen auch, kann es zur unkontrollierten Proliferation der betroffenen Zelle kommen – die Grundlage für die Entstehung einer Krebserkrankung.
Personalisierte Medizin ist digital
Bei Roche arbeiten wir seit Jahrzehnten daran, dass jeder Patient zum richtigen Zeitpunkt die zu seiner individuellen Krebserkrankung passende Behandlung erhält. Entscheidend dafür ist das Zusammenwirken von Diagnostik und Pharmazie, welche durch Daten in einen intelligenten Zusammenhang gesetzt wird.
Digitale Technologien können jetzt die Gene eines Tumors untersuchen, potenziell krebsauslösende Veränderungen parallel testen und diese riesigen Mengen an Informationen speichern, ordnen, filtern, mit anderen Daten vernetzen, bewerten – und somit letztlich nutzbar machen. Die Digitalisierung wird damit zum Katalysator der Personalisierten Medizin: Patienten mit malignen Erkrankungen werden so mehr und mehr aufgrund ihrer spezifischen genetischen Veränderungen stratifiziert und im Sinne der Personalisierten Medizin behandelt.
Die moderne Onkologie erfordert die interdisziplinäre Zusammenarbeit von Medizin und Health-IT. Dieser kollaborative Weg ist bereits Realität: In dem 2017 eröffneten europäischen Foundation-Medicine-Labor in Penzberg, Roches Kompetenzzentrum für Personalisierte Medizin, entstehen umfassende Tumorprofile, die Onkologen bei der Auswahl einer wirksamen Behandlung für ihre Patienten unterstützen. Der Service FoundationOne®CDx analysiert mittels Next Generation Sequencing mehr als 300 krebsrelevante Gene auf alle vier genetischen Veränderungen: Basensubstitutionen, Insertionen/Deletionen, Genfusionen und Kopienzahlvariationen. Das Ergebnis: ein Report, der alle gefundenen Genmutationen und dazu passende Therapieoptionen sowie klinische Studien auflistet.
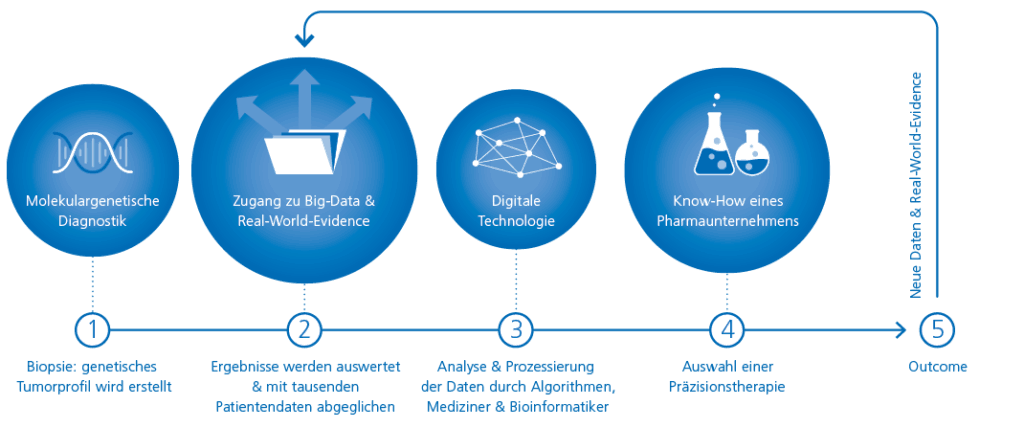
Quelle: Roche
Morgen: Nicht nur das Wo, sondern das Warum zählt
Und das ist erst der Anfang: Indikationsübergreifende Ansätze, die ausschließlich spezifische Mutationen eines Tumors berücksichtigen, stehen nun auch in der EU kurz vor der Zulassung, ebenso wie Krebsimmuntherapien, bei denen die eigenen Immunzellen des Patienten modifiziert werden. Maßgeschneiderte Krebsvakzine befinden sich bereits in der klinischen Prüfung. Es wird deutlich: Wir haben das Ende der Entwicklung noch lange nicht erreicht – vielmehr stehen wir gerade am Anfang einer neuen Generation revolutionärer Wirkansätze und Therapien in einer noch individuelleren, noch persönlicheren Personalisierten Medizin.
Eine individuelle Medizin ohne Kompromisse
Wird nun alles besser, schneller, wirkungsvoller und günstiger? Nein, sicher nicht, und vor allem nicht von allein. Die Digitalisierung und Personalisierung der Onkologie und der Medizin insgesamt ist ein Transformationsprozess, der uns viel Kraft, Investitionen und Geduld abverlangen wird. Ein Prozess, der zwar unaufhaltsam ist, aber nicht von allein in die Richtung verläuft, die uns allen nutzen wird.
Die Vision in der Onkologie: In zwanzig Jahren soll niemand mehr an Krebs sterben. Eine vernetzte, digitalisierte und Personalisierte Medizin ist dafür eine Grundvoraussetzung. Denn ohne die umfassende Nutzung von (molekularen) Daten zur Prävention, Früherkennung, zielgerichteten Therapie und Verlaufskontrolle sowie deren Integration mit weiteren Datenquellen ist dieses Ziel nicht zu erreichen. Zugleich helfen uns diese Daten dabei, neue prognostische Marker und Zielstrukturen zu finden sowie neue Wirkstoffe effektiver zu erforschen und schneller zum Patienten zu bringen.
Dazu müssen wir innovationsfreudig, wandelbar und mutig sein, vertraute Mechanismen in Behandlung, Forschung, Zulassung und Nutzenbewertung hinterfragen und zeitgemäß entlang der vorhandenen Evidenz anpassen. Dazu braucht es den Willen aller Beteiligten: von Pharmaunternehmen, Ärzten, Patienten, Kostenträgern und Gesetzgeber. Es braucht die Erkenntnis, dass wir im Kampf gegen Krebs – die Erkrankung, an der jeder Vierte von uns sterben wird – dasselbe Ziel verfolgen und den gemeinsamen Willen, ihm mit allen Mitteln entgegenzutreten. Initiativen wie die „Nationale Dekade gegen den Krebs“ sind deshalb ein wichtiger und notwendiger Schritt, um die Vision einer Zukunft ohne Krebstote Realität werden zu lassen. Digitale Technologien, molekulare Diagnostik und personalisierte Therapieoptionen sind diese Mittel. Jetzt gilt es, sie zu nutzen.■
EIN ENTSCHEIDENDER DREIKLANG: DIAGNOSTIK, PHARMAZIE UND HEALTH-IT
Um jedem Patienten ein längeres und besseres Leben zu ermöglichen, benötigen wir Kompetenzen jenseits klassischer Branchengrenzen. Als Pionier in der Personalisierten Medizin gehen wir bei Roche diesen Weg seit Jahrzehnten offensiv an. Diagnostik, Pharmazie und Biotechnologie arbeiten bei uns erfolgreich unter einem Dach. Individualisierte, präzise Krebsbehandlungen erfordern jedoch mehr als hochentwickelte Diagnostik und zielgerichtete Therapien. Die notwendigen Kenntnisse in der Health-IT bauen wir systematisch durch Allianzen aus. Durch die Akquisition von Foundation Medicine (FMI) und Flatiron Health stärken wir unser Know-how in der molekularen Diagnostik, der Vernetzung und Interpretation von Daten, sodass sie für die Therapie und in Forschung und Entwicklung nutzbar sind.
Autor/Autorin

Prof. Dr. Hagen Pfundner
Prof. Dr. Hagen Pfundner ist seit 2006 Vorstand der Roche Pharma AG und Geschäftsführer der Roche Deutschland Holding GmbH. Nach seinem Pharmaziestudium in Freiburg arbeitete Pfundner zunächst an den Universitäten Marburg und Kiel, bevor er 1992 seine Karriere bei Hoffmann-La Roche begann.
